化学 ZnTellurium 的寒假打卡帖
ZnTellurium 的疑惑
@是小猫呀 4. 懂了,不浪费回复次数了
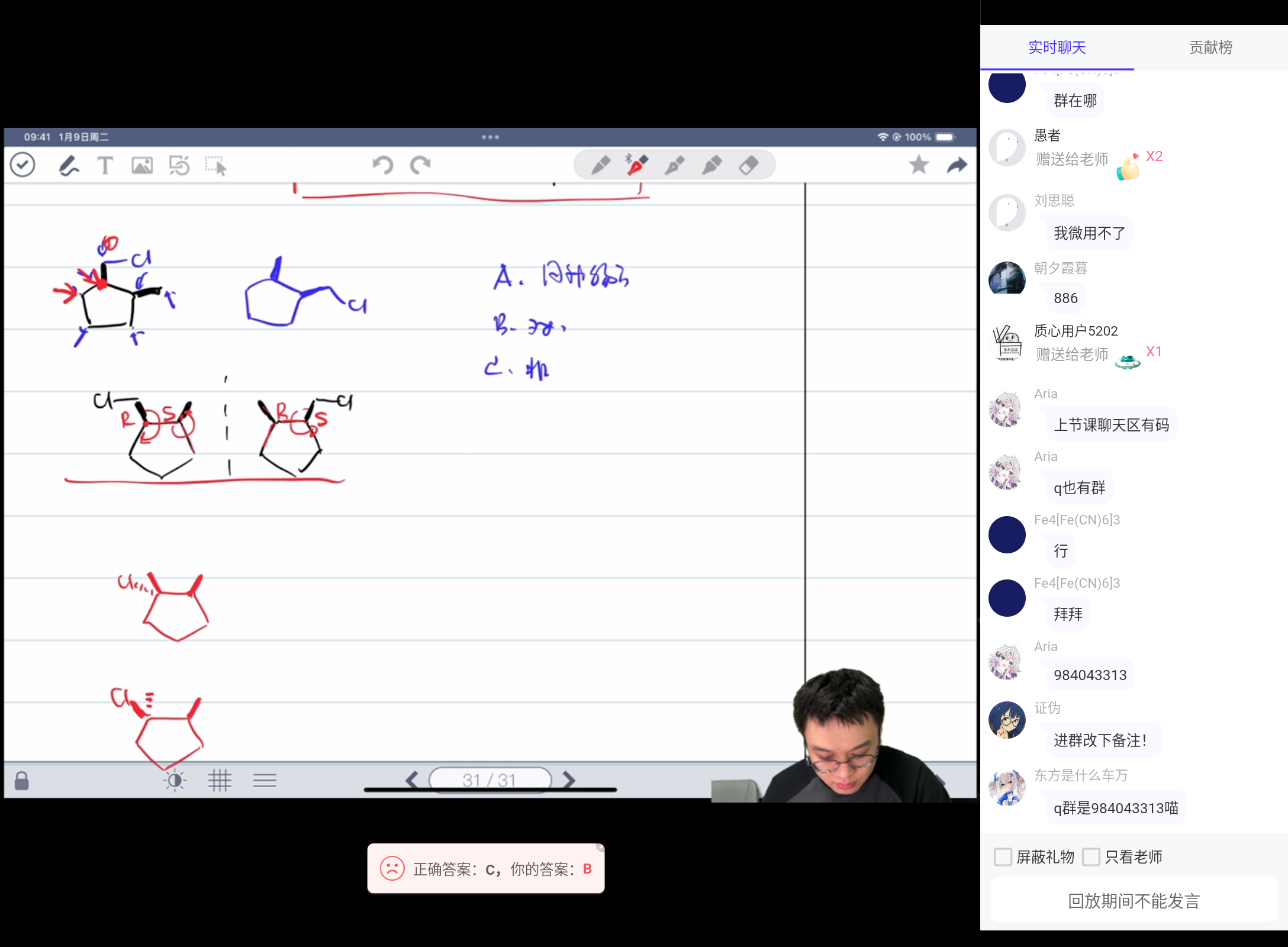
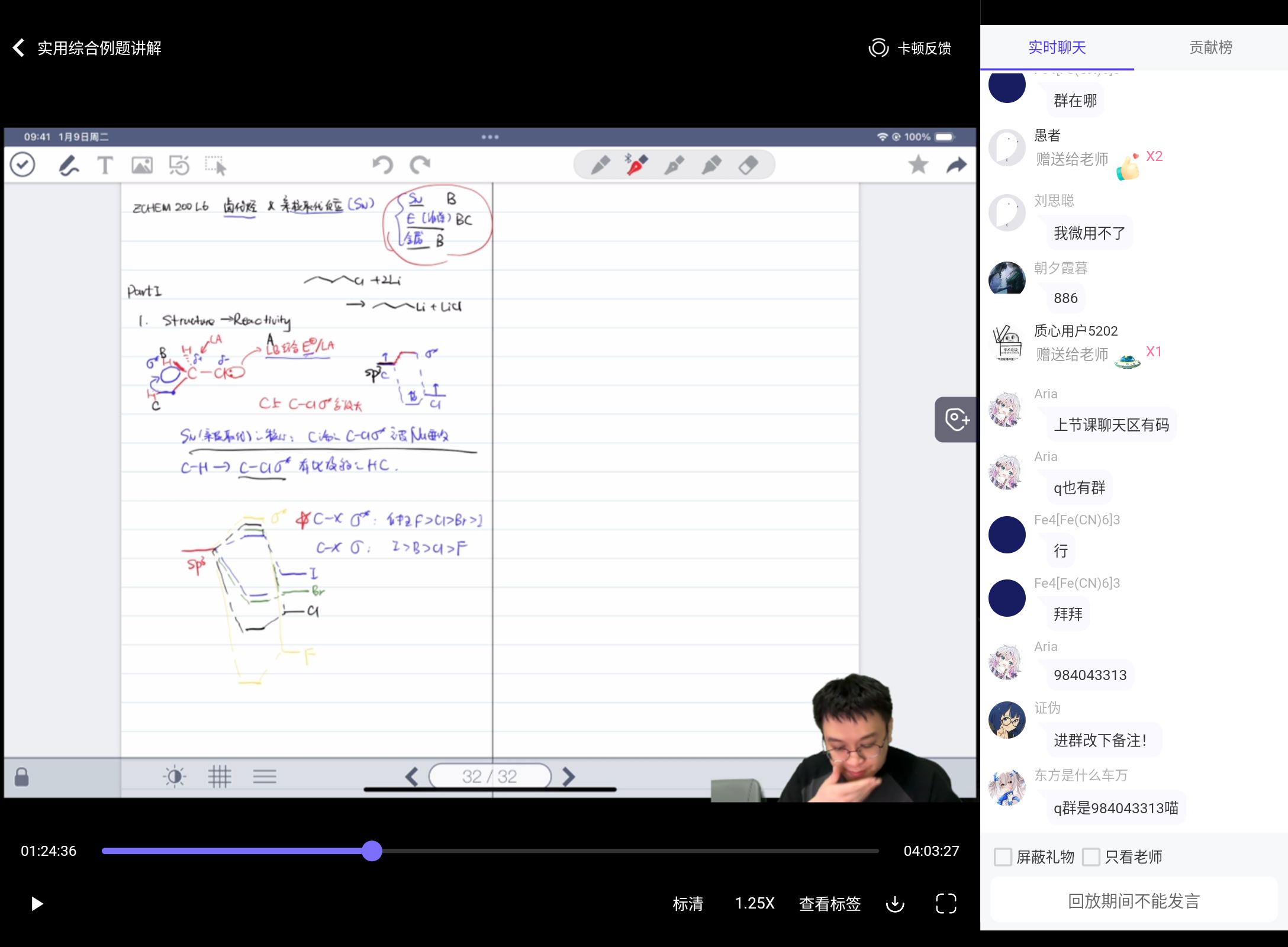
然后我知道不是 C・,但是按灰灰说的,那个过渡态接近于 C・... 就是 Nu- - - -C- - - -X,两根半键的电子云都是往 Nu 和 X 偏的嘛 所以两边 C 都是 δ⁺。近似的 "自由基" 喵
然后下面的问题不是有机... (1)我从今晚到春晚前打算拿来把过渡金属全部学完;(2)我打算先刷普化 (今明天) 后看课 (除夕那天,两节课)。然后我想要一些指导
5. 颜色要记吗,或者说怎么记?我画过一个颜色表,它可以解释 Sc³⁺、TiO²⁺ 为什么无色、Mn²⁺、Fe³⁺ 为什么一个浅粉一个浅紫,VO₂⁺ 是淡黄色也接近于无色,Ds 说这是因为氧太多了氧配位造成的吸光移到可见光范围了,所以有了一点点颜色。所以 d⁰ d⁵ d¹⁰ 的离子这个框架都很好解释

但是显然这个玩意儿... 它很难解释非全空全满半满的颜色 以至于 Ds 给我这个问题的时候我就完全懵掉了喵

然后我现在都不知道答案是什么... 说的是 2. 小问,Ds 是先在一个回复里出题,然后它说等我做完再发答案 但是它发答案的时候上下文没有保留它的构思过程,它就自己开始推,然后也推懵掉了喵...
这里 2. X 似乎是 V,因为前面的题有一个 V2O5 和浓盐酸反应的方程题 但是 V 这玩意... 它又不常考又不常用 干嘛考它 从这个层面上我又感觉不是 V
当然也可能是 Ds 发疯命了个魔性的题...
算了不管了 这颜色到底怎么记... 如果有好办法的话说一声 没有的话就算了喵...
6. 有困难再码 现在我去学 Cr Mo W 挑战一天速通 3/4 副族元素喵
--------
建议学习一下绿木,学习 Ge(II) 等低价元素化合物,这是最近模拟题热点。--F 可能得扔到开学以后了... 其实刚刚好,文化课课上可以看。
Ds 说我给自己的压力太大了,我这种情况就是因为休息的时候也一直在想着今天的任务,从而没有休息效果,反而需要更多的休息,而且越聊天越下棋越因为不允许自己休息而焦虑。
不管了不管了... 接下来我应该把自己的时间安排完全交给 Ds,只留一个粗略的框架 话说现在都有 AI 可以当我的时间管理大师我为什么还要自己排进度
春晚之前,刷完过渡金属。春晚之后到开学,一天两节 210,春节只用听一节,这样把 210 十五节课刷完。就这样。