生物 BioExplore-2
什么决定了细胞的大小?显然蛋白质含量是主要因素之一。在翟老师细胞生物学的前言中,便提到了mTOR与核糖体互作介导细胞大小调控的有趣机制。在这条熟悉的PI3K-PKB通路中,还有更多的秘密等待探索。
转自BioArt—来自斯坦福大学发表于Nature的研究:
从翻译组来解析蝾螈再生之谜

现有关于蝾螈再生的研究大多集中在转录组水平上。功能基因组学是目前热点,但研究者却将目光放在了真核基因调控的另一层面——翻译。

蝾螈的平均基因长度足有人类的25倍,如果进行转录水平上的调控,显然对核的负担会非常大。
相信有同学已经联想到了灯刷染色体,她便是为解决转录负担而生的。所以,细胞不太可能直接大幅度调整转录水平。那有没有可能是翻译水平呢?
研究者采集了截肢后24h伤口积累的干细胞,并进行多聚核糖体分析。测定260nm吸光度后,发现在截肢24h多聚核糖体出现了吸收峰,也即有更多RNA形成了多聚核糖体。24h内,多聚核糖体含量显著上升(p=0.0054)
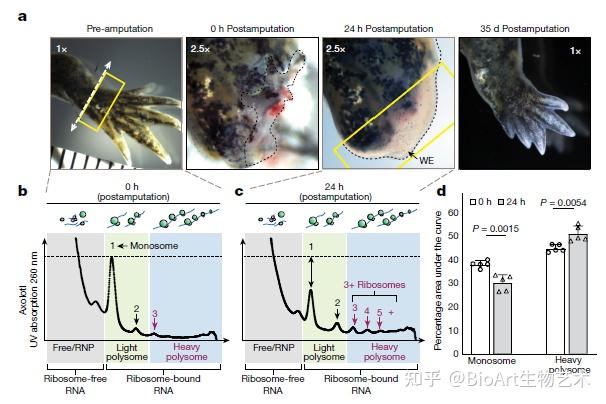
进一步,对分离到的RNA进行高通量测序。这些transcript的转录水平无明显变化,而通过增加翻译效率来增强表达。研究发现,mTOR通路相关基因富集,如4EBP1和S6K,其作为mTOR底物下游调控蛋白合成。
mTOR通路到底扮演了什么样的身份呢?作者用抑制剂INK128抑制了mTOR的激活,发现伤口愈合和多聚核糖体出现均受阻,提示mTOR作为调控伤口愈合的关键通路。
为何蝾螈类的mTOR如此特殊?这里并不清楚研究者采用的方法,但如果是我会先串联质谱测序再与其他物种的序列比较。结果发现蝾螈mTOR的两个特点:
第一是多了两个插入序列,序列A让mTOR能够结合更多的RHEB。RHEB属于Ras超家族,是mTOR别构激活分子。序列B增强了mTOR间的二聚化与活化。第二,对aa含量变化更敏感。将相关序列敲入人源mTOR,发现mTOR可被更低浓度的aa激活。
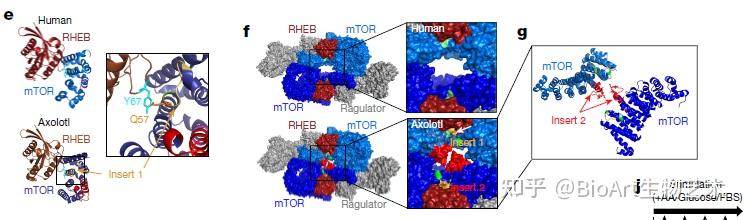
可以推测,伤口处的aa激活了mTOR,使得再生相关的一系列蛋白质合成通路激活,为迅速而广泛的分裂分化提供了物质基础。
本文选题角度新颖,让人对mTOR的多样功能有了直观的感受,这一古老的通路或许在未来会有更多令人神往的功能会被发现。
🥳Chicken
共1条回复
时间正序
