共4条回复
时间正序
- 时间正序
- 时间倒序
- 评论最多
伏行之混沌
1年前
2024-3-30 06:41:06
答案给的是由弱到强吗?如果是的话,A组就是比固定住苯环的能力大小,让他们能稳定共轭。B组,大概就是比较离域范围吧?(我很菜的,看看就行
1条评论 评论
- 1
李润钢
1年前
2024-3-30 08:40:24
按照art的说法,位阻增大后碱性增强,A组的负电荷都是跟三个苯环离域,但是位阻是2<3<1;至于B组,我想是因为一个苯环对负电荷离域的影响不如位阻带来的影响显著?
叠加态
1年前
2024-3-30 11:02:47
- A组答案酸性由弱到强吧。第一个太挤形成芳香对能量不利;第二个单有一个五元还好,但题目中有两个环并上去了,使其舍弃sp 3杂化而形成芳香性不是很有利,但较呢个最挤得肯定要好;最后一个可以形成sp2 以形成芳香性,对能量有利。
- B组由强到弱。我本以为是由弱到强😅,因为芳香离域范围增大了。然后觉得哪里不对,我又说不出来。就给你查了一下大本p 24页的酸性表,果然我错了😂。所以,我觉得位阻使其酸性降低(因为芳香性需是平面结构),这三个东西一定形成了芳香性,但都不如一个五元环时构像扭得舒服。所以有强到弱。
2条评论 评论

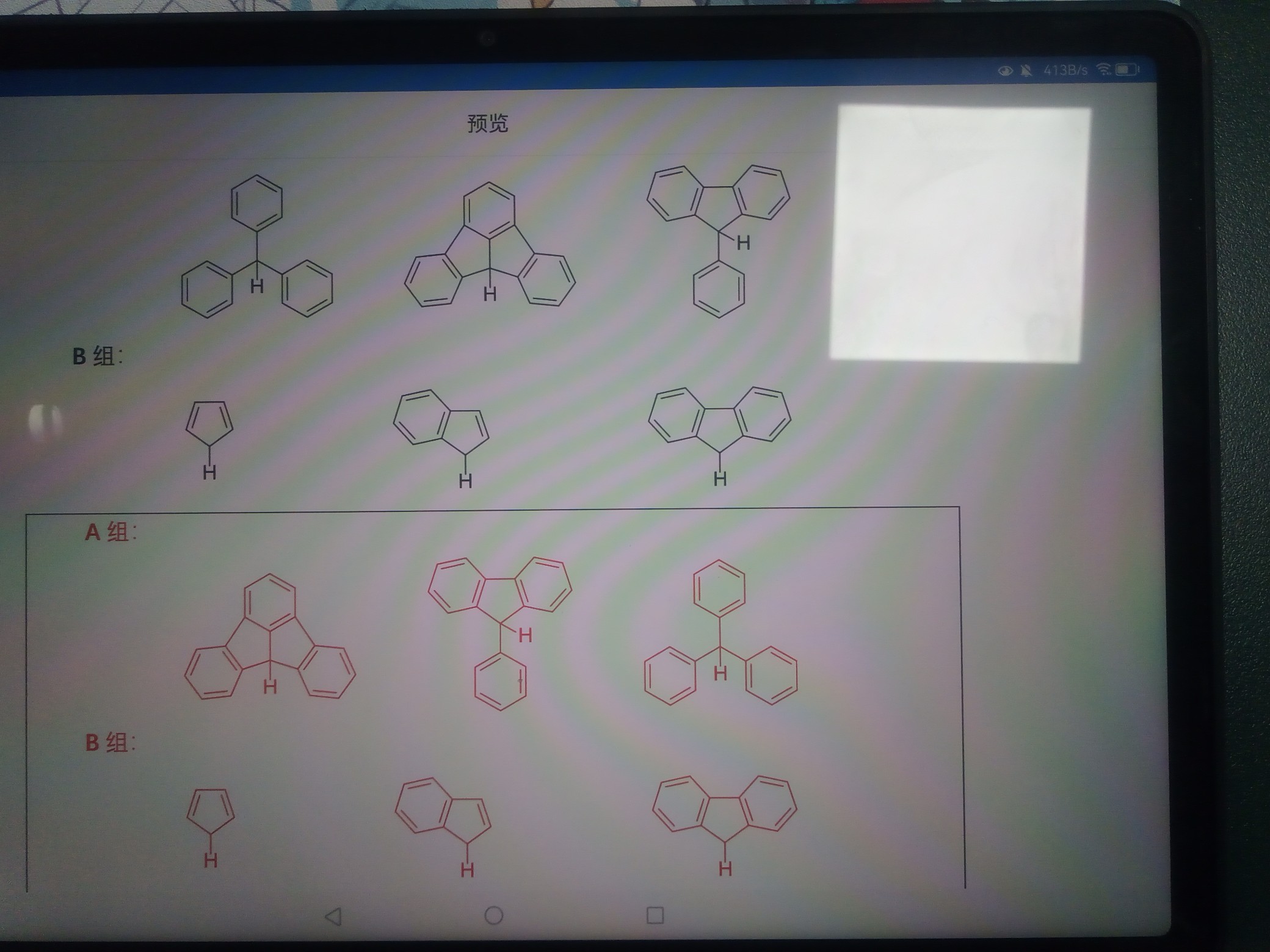 有没有大佬能解释一下为什么这两组物质的酸性排序是这样的?
有没有大佬能解释一下为什么这两组物质的酸性排序是这样的?